技術情報 -Technical Information
逆相固定相のアルキル基
逆相固定相のアルキル基:寝込んでいるのか?また資料との相互作用は?
逆相固定相のアルキル基はどんな状態で存在しているのでしょうか?
実験データに基づき考察しました。内容に対するどんなコメントでも大歓迎です。
今まであまり語られていないアルキル基の存在状態について議論できれば幸いです!
pdfファイルでご覧になりたい方はこちら pdf 1.37MB

水移動相条件で逆相カラムを用いた場合に、保持時間が減少することが知られています。 この保持の減少はアルキル基の寝込みが原因であるとの報告が1980年来、多くの研究者により発表されてきました。 しかし、長江らは2000年に水移動相条件での保持の減少はアルキル基の寝込みではなく、充填剤細孔からの水の抜け出しが原因であると発表し、 さらにこの抜け出しは毛管作用で起こっていることを明らかにしました。以前言われていたアルキル基の寝込みについて、実はどうなのだろうかと考え、 このようなタイトルの考察をしました。まず、有機溶媒の溶媒和についての基礎的な考察から行い、 メタノール・水、テトラヒドロフラン・水移動相の分離から、固定相の状態について考察しました。
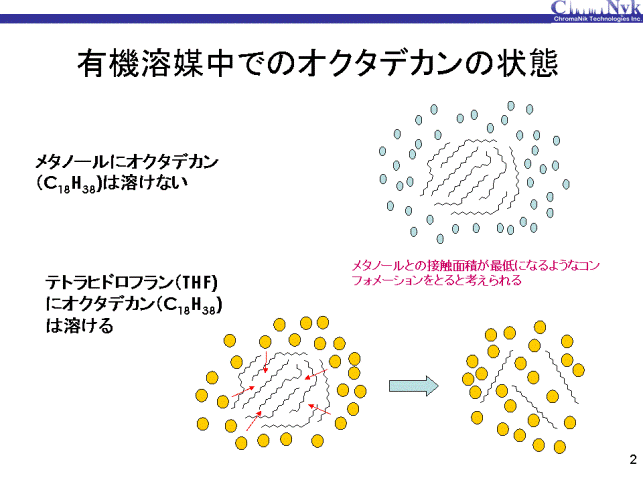
C18固定相のオクタデカン単体は有機溶媒に溶解するかどうかを考えました。 メタノールはヘキサンですら混ざらなく、炭素数18のオクタデカン(C18H38)はほとんど溶けないと考えられます。 テトラヒドラフラン(THF)はどうでしょうか。THFは多くの化合物を溶解することができ、 以前からゲルパーミションクロマトグラフィ(GPC)の移動相として用いられています。 溶解力の高いTHFはオクタデカンを溶かすことができます。
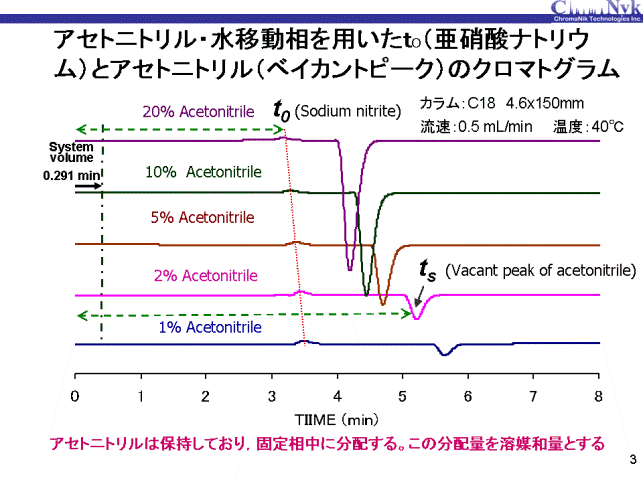
C18カラムに水移動相を用いると、有機溶媒は保持します。1%のアセトニトリル(アセトニトリル/水=1:99)の移動相を用いてもアセトニトリルは保持します。 この図では0.1%亜硝酸ナトリウム水溶液を注入しており、アセトニトリルはマイナスにピークが出現するベイカントピークになります。 移動相の有機溶媒濃度の増加につれ保持は小さくなりますが、それでも保持しております。有機溶媒が保持していることは、 固定相に有機溶媒が分配していること意味しています。それぞれの移動相には一定量の有機溶媒が含まれており、 また保持(k)の値により移動相中と固定相中の有機溶媒量の比が決定されるため、この両値から固定相中の有機溶媒の分配量を求めることができます。
k=(固定相中の有機溶媒量)/(移動相中の有機溶媒量)
また、t0として用いた亜硝酸ナトリウムの溶出時間は短くなっています。 このことは、固定相に分配(溶媒和)された有機溶媒も固定相の一部として働いており、 溶媒和量の増加に伴い固定相の容量も増えたことが原因だと推察されます。
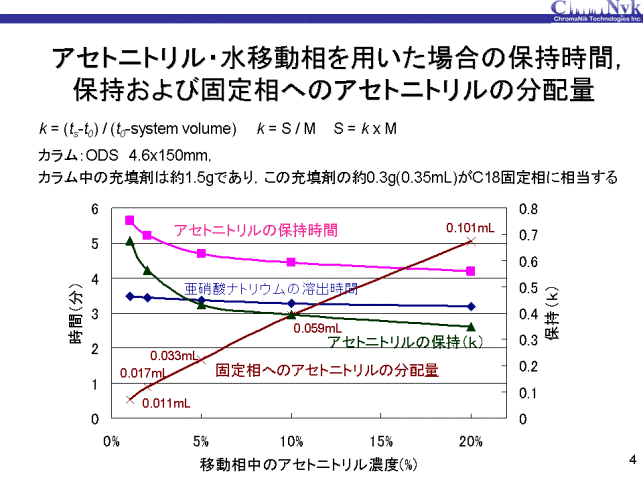
アセトニトリルの保持時間(ピンクの線)と亜硝酸ナトリウム(t0、青の線)の溶出時間から、 それぞれの移動相でのアセトニトリルの保持(緑の線)が計算されます。それぞれの移動相はアセトニトリル濃度が決まっているため、 移動相中に存在するアセトニトリル量に保持係数を乗じた値が固定相中に分配しているアセトニトリル量になります。
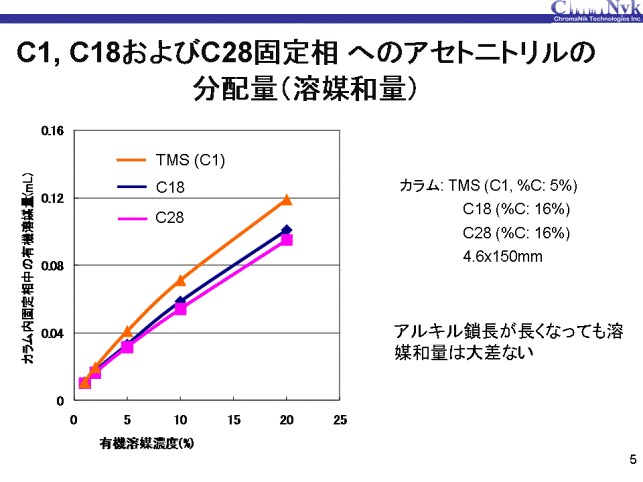
C1 (TMS)、C18およびC28固定相を用いた場合のアセトニトリルの有機溶媒和量を示します。 有機溶媒の濃度の異なる水溶液移動相での保持から溶媒和量を求めました。 移動相中の有機溶媒の増加に伴いそれぞれのベイカントピークの保持も小さくなるため、 誤差を顧慮し信頼の置けるデータとして有機溶媒量を20%までとしました。 アセトニトリルの溶媒和量はアルキル鎖長の異なる固定相でも、全てほぼ同じ値になりました。
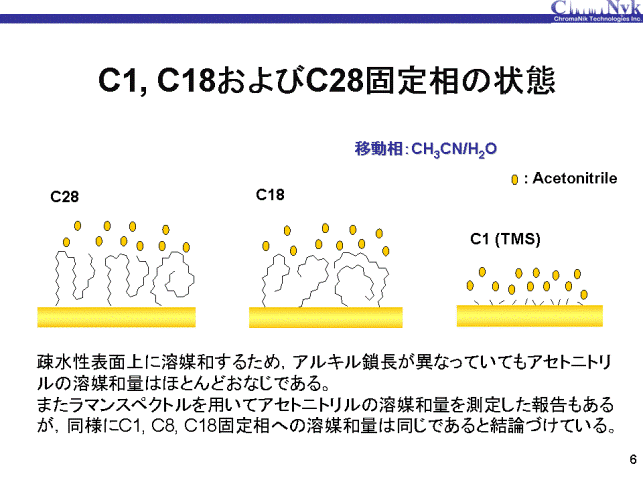
アセトニトリルにオクタデカン(C18H38)は溶けないため、C18およびC18固定相はアルキル基が固まった状態であると考えられます。 また、それぞれの溶媒和量がほぼ同じであるため、アセトニトリルは固定相表面上に溶媒和しており、 アルキル鎖長が異なっていても同じ疎水性の表面であれば、同量の溶媒和になると考えられます。
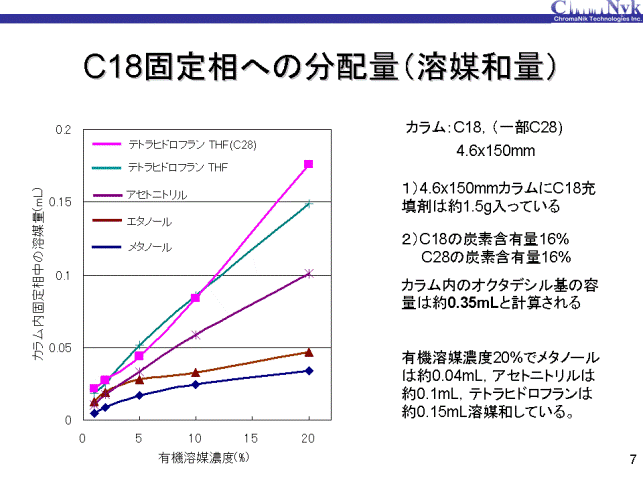
C18固定相を用いた場合の有機溶媒和量を示します。それぞれの有機溶媒の濃度の異なる水溶液移動相での保持から溶媒和量を求めました。 また、C28固定相のTHF・水を用いた場合を参考値として追加しました。 移動相中の有機溶媒の増加に伴いそれぞれのベイカントピークの保持も小さくなるため、 誤差を顧慮し信頼の置けるデータとして有機溶媒量を20%までとしました。 メタノール・水移動相ではメタノールの溶媒和量はあまり多くありませんが、 THF・水移動相ではTHFの溶媒量は非常に多く、20%濃度でメタノールの約4倍量でした。また、この図には示しておりませんが、 C28固定相のメタノール、エタノールおよびアセトニトリルの溶媒和量はC18固定相とほぼ同じ値になりました。
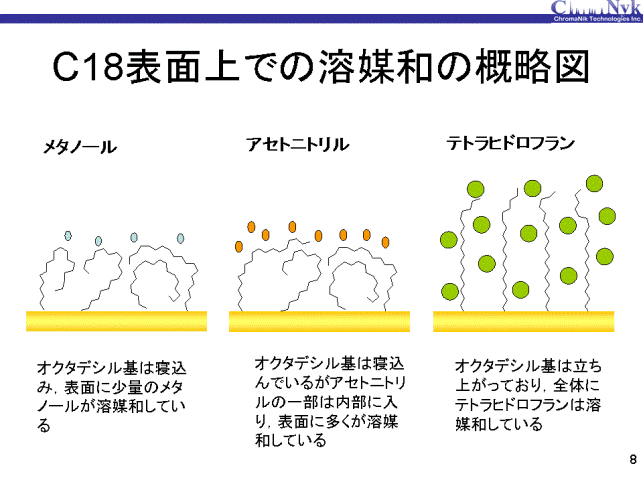
有機溶媒和量の結果とオクタデカンのそれぞれの有機溶媒への溶解性から、 メタノールのC18固定相への溶媒和はアルキル基が固まった(寝込んだ)状態で、 表面にメタノールがOHを外に向け存在していると考えられます。 また、THFは濃度が低く溶媒和量が少ない場合にはアルキル基は固まった状態であると考えられますが、 ある程度の溶媒和量からはアルキル基固定相内部まで入り込んだ状態になると推察されます。 アセトニトリルの溶媒和量はメタノールとTHFの中間状態であるため、アセトニトリルは多くは表面に存在していますが、 一部は固定相内部に入り込んでいると考えられます。
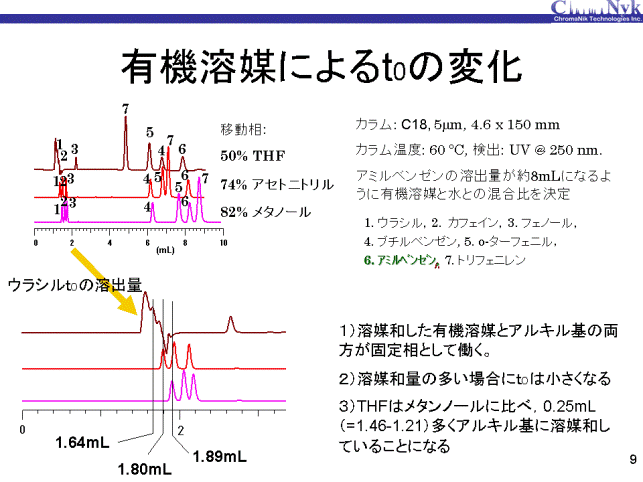
C18カラムのt0の溶出時間(溶出量)の変化量から、固定相の容量変化量(溶媒和量)を求めることができます。 アミルベンゼンの保持が8分程度の移動相ではウラシルはほとんど保持せず、ほぼt0であると考えられます。 50%THF(THF/水=50:50),74%アセトニトリル(アセトニトリル/水=74:26)および82%メタノール(メタノール/水=82:18)を移動相として用いた場合の ウラシルの溶出量はそれぞれ1.64mL、1.80mLおよび1.89mLとなりました。この値から、82%メタノールに比べ、 74%アセトニトリルでは固定相内への有機溶媒の溶媒和量が0.09mL多いことを意味しており、50%THFは0.25mL多いことになります。
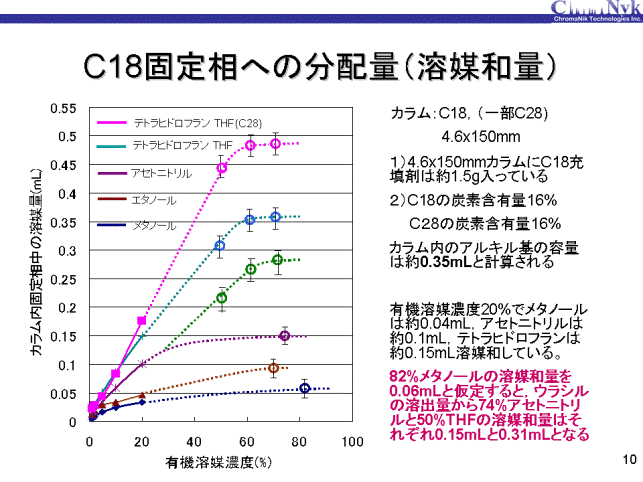
82%メタノールのC18固定相への溶媒和量を0.06mLと仮定し、前スライドのデータから74%アセトニトリルおよび50%THFの溶媒和をプロットしました。 また、同様に70%エタノールの溶媒和量も求め、プロットしました。 さらに、C18固定相とC8固定相、C28固定相の50%THF、60%THFおよび 70%THF移動相でのウラシルの溶出量を測定し、74%アセトニトリルのウラシルの溶出量の差から、 THFの溶媒和量を求め、プロットしました。THF・水移動相では60%まで溶媒和量は直線的に増加し、その後フラットになりました。
C18固定相へのメタノールの溶媒和量は非常に少なく、メタノール100%でも0.07mL程度だと考えられます。 カラム内のC18アルキル基のみの容量が0.35mLと計算され、メタノールは固定相としてのアルキル基のみの容量の1/5程度しか溶媒和しないことになります。 この程度の溶媒和ではC18アルキル基は固まった(寝込んだ)状態であると推察されます。 また、THFの場合は60%濃度ですでにアルキル基の容量と同じ0.35mL程度溶媒和しており、THFはほぼアルキル基全体に溶媒和し、 アルキル基は立ち上がった状態になっていると推察されます。
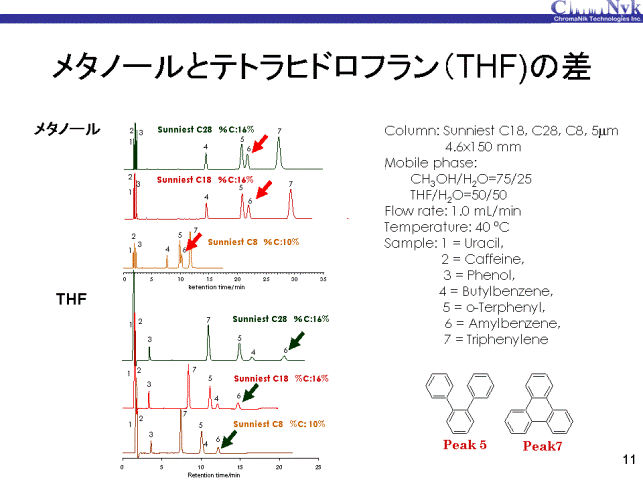
炭素含有量16%のC28固定相、同じく炭素含有量16%のC18固定相および炭素含有量10%のC8固定相を用いて、 メタノール/水=75:25移動相と、THF/水=50:50移動相を用いて標準試料の分離比較を行いました。 アミルベンゼンの保持を比較しますと、メタノールの場合にはC28とC18は変わりません。 つまり炭素含有量が同じであるため、アルキル基が固まった固定相では容量や状態も同じであると考えられます。 C8は炭素含有量がC28やC18の6割であるため、アルキル基が固まった状態では半分の保持になったと考えられます。
THFの場合には同じ炭素含有量でもC28の方がC18よりも保持は大きくなりました。 これはTHFの固定相内への溶媒和量がC18よりもC28 の方が多いため、固定相の容量がC28の方が大きいためであると考えられます。 メタノール・水移動相とTHF・水移動相でアミルベンゼンの保持挙動が大きく異なるのは固定相の状態(溶媒和量)が異なっているためだと推察されます。
また、THF・水移動相では立体選択性(Steric selectivity)を示すo-ターフェニルとトリフェニレンの溶出順序がメタノール・水移動相と逆になっており、 さらに保持はブチルベンゼンより小さく、全く異なった分離になりました。 メタノールやアセトニトリルを移動相の有機溶媒として用いた場合にはo-ターフェニルとトリフェニレンの溶出順序は同じですが、 THFを用いた場合に溶出順序が逆になりました。この原因は、有機溶媒により固定相の状態つまり溶媒和量が異なり、 THFでは固定相への溶媒和量が非常に多く固定相自体が大きく変化しているとことであると推察されます。
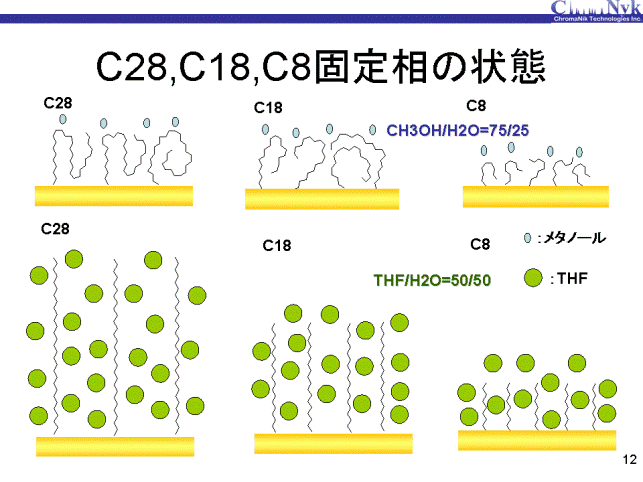
メタノール・水=75:25移動相とTHF・水=50:50移動相条件下での、C28、C18およびC8固定相の状態を示します。 メタノールはアルキル基が固まった状態の表面に溶媒和しているのに対し、THFはアルキル基全体に溶媒和してアルキル基が立ち上がり、固定相が膨らんでいると考えられます。 また、C28はC18より4割程度多くTHFを溶媒和していると考えられます。
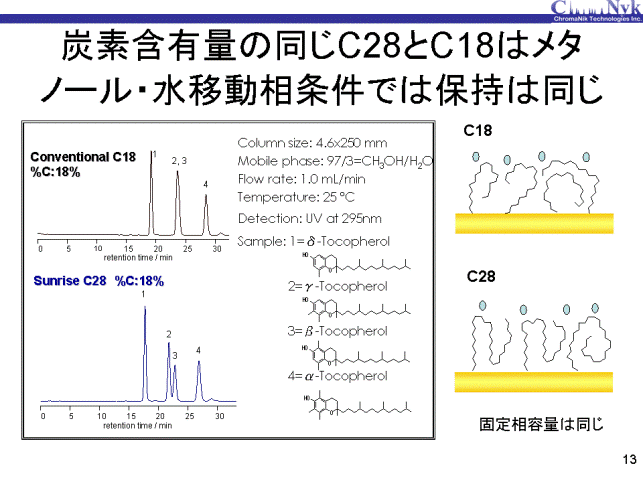
炭素含有量18%のC28固定相、同じく炭素含有量18%のC18固定相を用いて、メタノール/水=97:3移動相を用い、ビタミンE(トコフェロール)分離を行いました。 C18は2番・3番の構造異性体であるβ-トコフェロールとγ-トコフェロールを分離することはできませんが、C28は分離しております。これはアルキル鎖長が異なるためであり、 アルキル鎖長の長いC28はメチル基の位置を認識できたと考えられます。保持時間はC18とC28ではほとんど同じでした。 つまり、炭素含有量が同じであるため、固まった状態での固定相が同じ容量になり、メタノール溶媒和が表面に同じように起こっておるためだと考えられます。
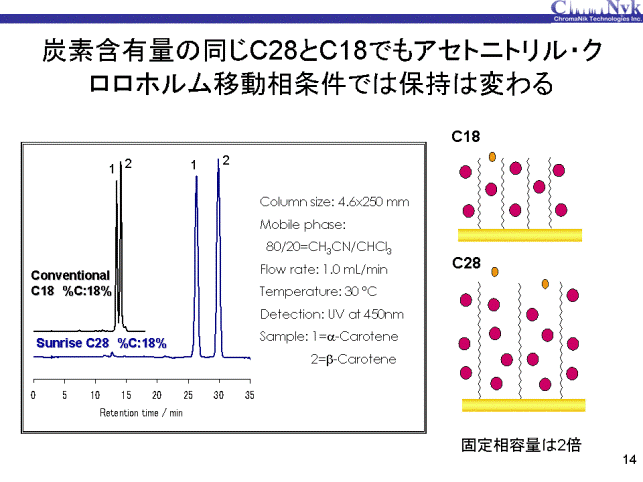
トコフェロールよりさらに脂溶性の高いカロテンの分離を、同様にC18とC28で比較しました。移動相はアセトニトリル/クロロホルム=80:20を用いました。 クロロホルムはTHFよりさらに疎水性が高く、溶媒和量はTHF以上になると考えられます。したがいまして、溶媒和量の多いC28はC18に比べ保持が2倍になったと考えられます。 α-,カロテンとβ-カロテンの分離はC28の方がよく、これはトコフェロール同様アルキル鎖長が長いためであると考えられます。 カロテンの分子の大きさはC18(ステアリル基、2.5nm)より大きく、1本のC18鎖だけではカロテン分子全体に相互作用できないのに対し、 C28はカロテン分子より長いため、C28鎖1本でカロテン分子全体に相互作用できるため分離が良くなったと推察されます。
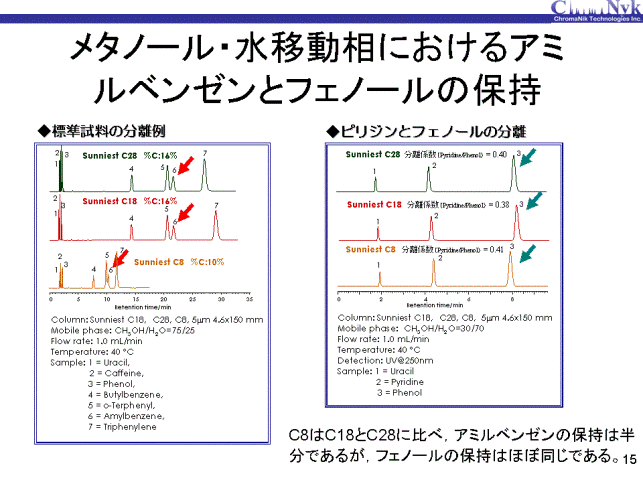
メタノール/水=75:25移動相を用いたアミルベンゼンの保持はC28とC18はほぼ同じで、 C8がその半分でしたが、極性が比較的高いフェノールの保持はどの固定相でもほとんど差がありませんでした。 メタノール/水=30:70移動相を用いて、フェノールの保持を大きくして差を比較したところ、 メタノール/水=75:25移動相と同様に、ほとんど同じ保持時間を示しました。 高極性化合物のカフェインはシリカ表面のシロキサン結合やシラノール基の影響を受け保持は大きく変化します。 しかしフェノールはシリカ表面の影響を受けず、保持はほとんど変わらないため、 シラノール基との相互作用である水素結合性のパラメータとしてカフェインとフェノールの分離係数が用いられています。 ではなぜアミルベンゼンは炭素含有量の低いC8で保持が半分になるのに対し、フェノールの保持は同程度なのでしょうか?
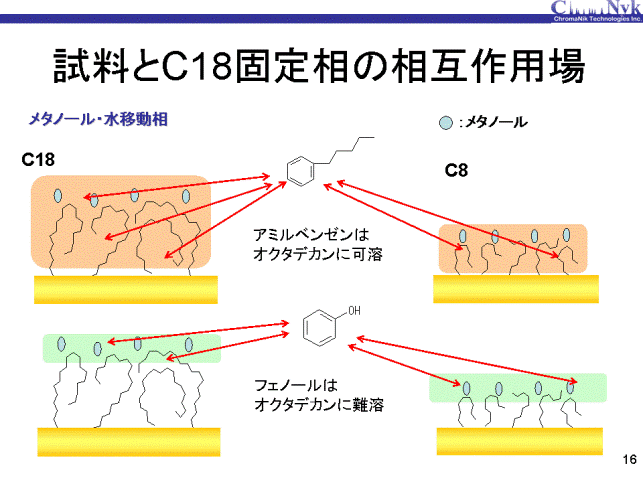
>アミルベンゼンとフェノールでは固定相として働くアルキル基の場所に差があると考えます。 アミルベンゼンは疎水性が高く、オクタデカン(C18H38)に可溶ですが、フェノールは極性が高いため、オクタデカンに難溶です。 したがってアミルベンゼンはC18やC8固定相の全体で相互作用していると考えられるのに対し、 フェノールは溶媒和しているそれぞれの固定相の表面で相互作用していると考えられます。 このように考察すれば、フェノールの保持がどの固定相でも同じであることが説明できます。
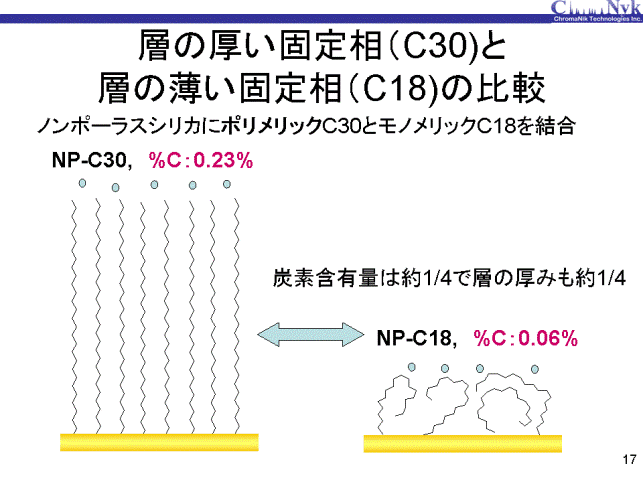
固定相の相互作用場の差があるかどうか調べるために、無孔性シリカにC30(3官能性トリアコンチルシリル基)を水を加えてポリメリック状態で、 結合蜜度が最大になるように結合させたNP-C30と、C18を無水条件でモノメリック状態で結合したNP-C18を調製しました。 炭素含有量はそれぞれ0.23%と0.06%となり、それぞれの固定相は図に示すようになっており、メタノール・水移動相での固定相容量は約4倍の差があると考えられます。 NP-C30固定相は結合密度が非常に高ため、固定相が固まった状態でもかなりのトリアコンチル基(C30)は立ち上がっていると推察されます。 今まで示しましたC28固定相はモノメリックC28ですので、結合密度はNP-C30と比べ半分以下であり、NP-C30とはまったく異なるものです。
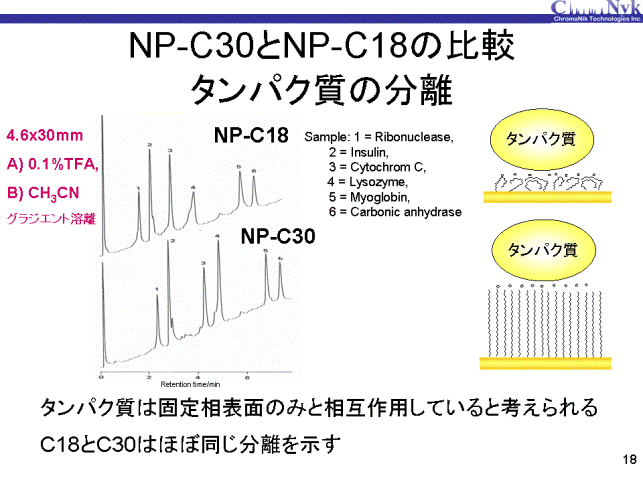
NP-C30とNP-C18を内径4.6mm、長さ30mmのショートカラムに充填し、タンパク質の分離を比較しました。両固定相とも同様な分離が達成されました。 タンパク質は巨大分子であり、通常のC18、C8およびC4固定相でもほとんど同じ分離が達成されます。 つまり固定相の表面で相互作用すると考えられています。NP-C18もNP-C30も固定相表面で相互作用しているため、ほぼ同じ分離になりました。
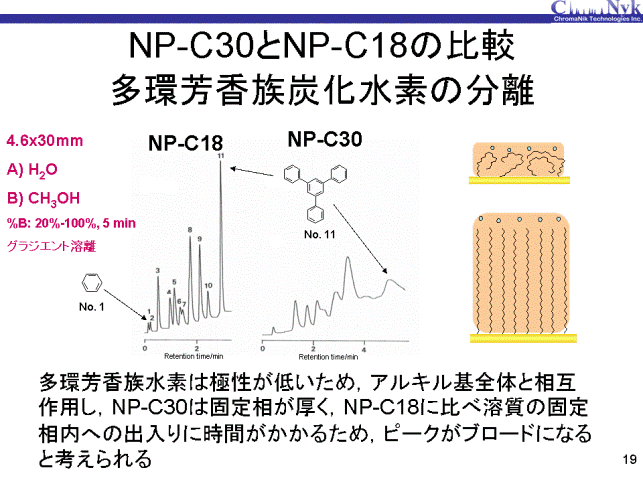
多環芳香族炭化水素を試料として、メタノール20%から100%を5分間で行うグラジエント条件で分離比較しました。 NP-C18は全ての成分でシャープなピーク形状ですが、NP-C30は保持が大きいほどピークはブロードになりました。 疎水性の高い多環芳香族炭化水素の分離ではアルキル基全体が固定相として働きます。NP-C18は一般的なC18とほぼ同じ固定相ですので、 分配平衡は瞬間的に起こっており、問題なく分離できますが、NP-C30は結合密度が高く固定相容量が約4倍であり、 疎水性で嵩の高い化合物はこのC30固定相内部に入り込んで固定相から抜け出るのに時間がかかるため、ピーク幅が広がったと考えられます。
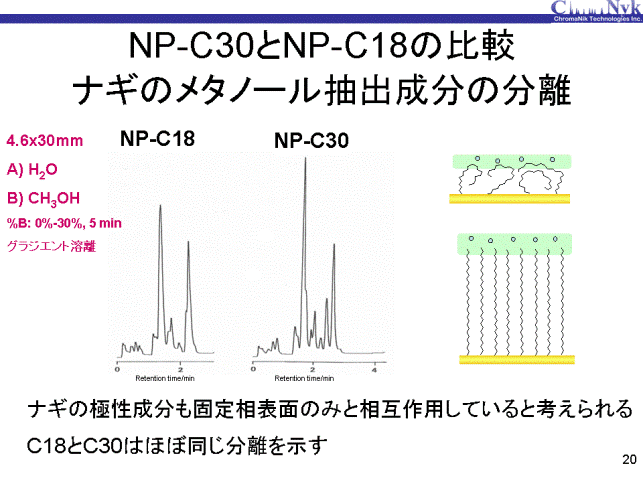
ナギ(植物)のメタノール抽出物をメタノール0%から30%までを5分間の条件でグラジエント溶離し、分離比較しました。 メタノール組成が15%までにほとんど溶出しており、高極性化合物の分離例です。分離はNP-C30の方がよく、 分離ピーク数も多いのですが、ピーク幅はNP-C30とNP-C18はほぼ同じでした。 前スライドの多環芳香族炭化水素はNP-C30では非常にブロードなピークになりましたが、ナギの極性成分はシャープなピークでした。 これはタンパク質と同様に固定相表面との相互作用であると考えるとつじつまが合います。
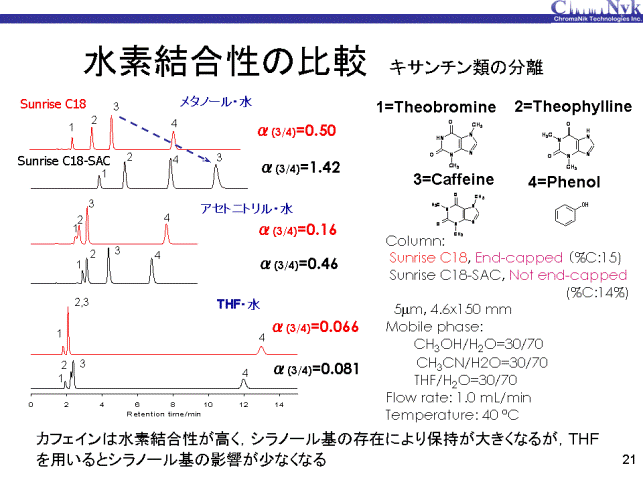
Sunrise C18-SACはシラノール基を残しており、Sunrise C18はSunrise C18-SACにTMS(トリメチルシリル化)のエンドキャップを施しています。 両固定相の差はシラノール基の有無です。メタノール/水=30:70,アセトニトリル/水=30:70とTHF/水=30:70移動相を用い、 テオブロミン、テオフィリン、カフェインおよびフェノールの分離を比較しました。 メタノール・水移動相ではシラノール基を残していることによりカフェインの保持が2.5倍大きくなり、 さらにフェノールとの溶出順序が逆転し、残存シラノール基の影響が大きく分離に反映されています。 この結果が示すように、メタノール・水移動相におけるカフェインとフェノールの分離係数(α(3/4))は水素結合性のパラメータとして広く知られております。 一方、THF・水移動相ではカフェインの保持はフェノールに比べ、非常に小さく、残存シラノール基による影響は認められるものの、 メタノール・水移動相に比べ残存シラノール基の影響は非常に少ないと言えます。水素結合性を示すカフェインとフェノールの分離係数は、 メタノール・水移動相に比べTHF・水移動相では極端に小さく、水素結合性(シラノール基との相互作用)はTHFを用いることにより減少してしまいます。 アセトニトリル・水移動相はメタノール・水移動相とTHF・水移動相の中間的な挙動を示しました。 この現象はスライド7の有機溶媒濃度30%の時の溶媒和量の関係に一致していると思われます。
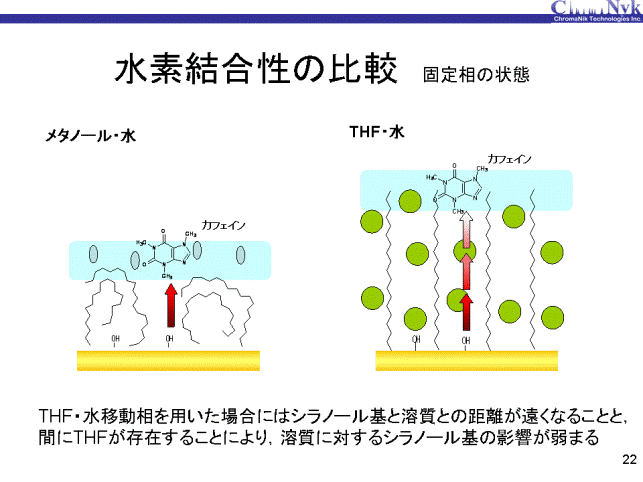
カフェインとシラノール基との相互作用(水素結合性)の状態を示します。 メタノール・水移動相ではカフェインはアルキル基が固まった固定相の表面に存在し、シリカ表面上のシラノール基の影響を受けています。 一方、THF・水移動相ではTHFが固定相内部に存在し、アルキル基はある程度立った状態になっており、この固定相の表面にカフェインが存在しています。 この場合、カフェインとシリカ表面のシラノール基との距離が長くなることと、 その間にTHFが存在することにより、シラノール基の持つ水素結合性が弱められると推察されます。
